Veterinaria (Montevideo), 2026 62, (225), https://doi.org/10.29155/VET.62.225.7
Reporte de caso
Flebitis irritativa y necrosis de vena cefálica, piel y tejido subcutáneo debido a extravasación de propofol en un canino adulto de raza york-shire terrier
Irritative phlebitis and necrosis of the cephalic vein, skin, and subcutaneous tissue due to propofol extravasation in an adult yorkshire terrier
Flebite irritativa e necrose da veia cefálica, pele e tecido subcutâneo devido à extravasação de propofol em um cão yorkshire terrier adulto
Claudia de Aurrecoechea1 https://orcid.org/0000-0003-4994-1226
Ignacio Fagúndez1 https://orcid.org/0009-0004-7579-309X
1Facultad de Veterinaria, Universidad de la República. Autor para correspondencia: cdeaurrecoechea@gmail.com
Cómo citar este artículo:
de Aurrecoechea, C., & Fagúndez, I. (2026). Flebitis irritativa y necrosis de vena cefálica, piel y tejido subcutáneo debido a extravasación de propofol en un canino adulto de raza yorkshire terrier. Veterinaria (Montevideo), 62(225), e20266222507. https://doi.org /10.29155/VET.62.225.7
Resumen
Se realizó una intervención menor de rutina (profilaxis dental) en un paciente canino de 3 años sin complicaciones, excepto por la infiltración de un catéter de acceso venoso periférico colocado en la vena cefálica. A las 24 horas posquirúrgicas, la tutora del animal relató que el paciente comenzó con una claudicación de apoyo que se fue agravando con los días hasta evidenciarse una necrosis de piel y subcutánea coincidente con la zona de colocación del catéter. Luego del manejo de la herida, se le dio de alta sin complicaciones, a excepción de una leve retracción de piel en la zona cicatrizal.
Palabras clave: Necrosis cutánea, Linfadenitis, Radio, Miositis, Staphylococcus aureus.
Abstract
A routine procedure (dental prophylaxis) was performed in a 3-year-old canine patient. The intervention was uneventful except for the infiltration of a peripheral venous catheter placed in the cephalic vein. Twenty-four hours after the procedure, the patient’s owner reported the onset of weight-bearing lameness in the affected limb, which progressively worsened over the following days. Clinical examination revealed necrosis of the skin and subcutaneous tissue, coinciding with the catheter placement site. Following the implementation of a local wound management plan, the patient showed favorable recovery and was discharged, with only a mild cutaneous retraction at the cicatricial area as a sequela.
Keywords: Cutaneous necrosis, Lymphadenitis, Radius, Myositis, Staphylococcus aureus.
Resumo
Foi realizada uma intervenção de rotina (profilaxia dentária) em um canino de 3 anos de idade, a qual transcorreu sem complicações, exceto pela infiltração de um cateter de acesso venoso periférico colocado na veia cefálica. Vinte e quatro horas após o procedimento, a tutora do animal relatou o aparecimento de claudicação de apoio no membro afetado, que se agravou progressivamente nos dias seguintes. Ao exame clínico, evidenciou-se necrose de pele e tecido subcutâneo, coincidente com a região de colocação do cateter. Após a implementação de um plano de manejo local da ferida, o paciente apresentou evolução favorável e recebeu alta, apresentando como sequela apenas uma leve retração cutânea na área cicatricial.
Palavras-chave: Necrose cutânea, Linfadenite, Rádio, Miosite, Staphylococcus aureus.
Fecha de recibido: 10/09/2026
Fecha de aceptado: 23/02/2026
Introducción
Las extravasaciones de drogas en el tejido perivascular son relativamente frecuentes en medicina veterinaria, pero las necrosis provocadas por estas no lo son tanto o se desconoce su prevalencia debido a la escasa información, hay reportes de casos sobre todo relacionados a extravasación de quimioterápicos, líquido de contraste para imagenología y vasopresores (Errante, 2023; Le & Patel, 2014; Vasquez et al., 2025). Por el contrario, se describen en detalle las complicaciones tanto locales como sistémicas asociadas al uso de anestésicos locales y su manejo específico (Fischer & Martin-Flores, 2024).
La prevalencia de extravasaciones de anestésicos con datos relevados en medicina humana es muy baja, existe información poco contundente extraída de los prospectos de las drogas utilizadas, que son menos de 1:10 000 pacientes humanos en propofol, no se encontraron datos concretos en caninos, excepto por reportes de casos y relatos de casos relacionados a complicaciones por catéteres endovenosos, la flebitis es la más prevalente (Simpson & Zersen, 2022). Debido a la molestia provocada por la inyección de propofol en algunos pacientes, se relatan algunas modificaciones en los excipientes del propofol para evitar el dolor en el sitio de inyección, incluso se relata la creación de drogas que no contengan excipientes de origen animal para utilizar en pacientes humanos veganos (Mahajan et al, 2006; Minghella et al., 2010), ya que es considerado un agente irritante y no un agente formador de vesículas como lo es el tiopental.
Las drogas utilizadas en anestesia general que pueden provocar irritación —y lesiones más severas como necrosis de piel y tejidos subcutáneos— son diazepam, etomidato, tiopental, propofol, fluidos utilizados para fluidoterapia como dextrosa, adrenalina, entre otros fármacos, como antibióticos que incluso han llevado a la elaboración de guías para el manejo de estas complicaciones (Garrigues et al., 2019). Las lesiones mayoritariamente descritas van desde irritación de los tejidos, necrosis con pérdida de tejido, claudicación de distintos grados hasta la necrosis del miembro, que debe ser seguida de una amputación (Carrillo et al., 2015).
Desde el punto de vista de su clasificación, estas heridas no se clasifican específicamente, sino que son tratadas del mismo modo que las heridas por quemadura química. Los tratamientos descritos para estos casos van desde la infiltración de suero fisiológico en la zona, inyección de antídotos que disminuya la actividad del fármaco derramado, aplicación de frío y manejo de heridas según la gravedad (Bohling & Henderson, 2006). La cicatrización esperable en este tipo de heridas es denominada cicatrización por segunda intención, produciéndose lo que se denomina tejido de granulación, debido a sus características, que le dan un aspecto granular: neovascularización, humedad, agregación plaquetaria, migración de células inflamatorias y reparadoras (neutrófilos, macrófagos y fibroblastos). Este tejido servirá de base para la generación de la cicatriz a través de los procesos reparatorios, produciéndose colágeno, migración de mayor cantidad de fibroblastos y división de epiteliales que formarán la piel. El objetivo de este reporte es compartir un caso con una prevalencia baja en cirugía y anestesiología veterinaria.
Reporte clínico
Se recibió un paciente canino macho sano de raza yorkshire terrier, entero, de 3 años y medio de edad, con peso de 1600 kg para la realización de una profilaxis dental o tartrectomía de rutina sumado a la extracción de una pieza dental decidua, concretamente el canino superior derecho o pieza dental n.o 104, con el objetivo de prevenir el desbalance de la microbiota oral (Flancman et al., 2018). El paciente se preparó para la cirugía, se depiló el miembro anterior derecho para la colocación de un catéter de venoclisis, marca SuperCath n.º 24G (amarillo), fijado a la piel de forma habitual con leukoplast mediante una corbata. A través de este se administró midazolam (0,35 mg/kg), tramadol (5 mg/kg) y ketamina (0,5 mg/kg) como preanestésicos, según referencias bibliográficas (Otero, 2012). El animal se sedó sin complicaciones y luego se indujo a la anestesia general con propofol[1] (bolo de 1 mg/kg a efecto de forma lenta). Al evidenciar que el animal no se inducía a la anestesia general al recibir la dosis total del fármaco se chequeó el catéter por una posible infiltración. Este se retiró y se colocó otro de la misma marca y calibre en la vena cefálica del otro miembro anterior. Finalmente se indujo con otro bolo de propofol a la mitad de la dosis y se lo intubó para el mantenimiento de la hipnosis con anestesia inhalatoria mediante isoflurano.[2]
El procedimiento tuvo una duración de 15 minutos y no evidenció complicaciones en parámetros clínicos básicos: SpO2 (saturación de oxígeno) del 100 %, promedios de frecuencia cardíaca de 95-120 latidos por minutos, frecuencia respiratoria de 12-14 respiraciones por minuto, temperatura rectal de 37,9-38,1 grados Celsius (°C) y presión arterial sistólica (PAS) promedio entre 110 a 160, diastólica (PAD) entre 60-95 y la media (PAM) entre 76 y 90 mmHg durante todo el procedimiento y hasta que se dio de alta luego de las dos horas de monitoreo posquirúrgico inmediato (Grubb et al., 2020). Se recomendó el uso de antibióticos profilácticos en base a espiramicina y metronidazol[3] una vez al día durante 5 días y dipirona jarabe[4] a dosis 25 mg/kg cada 8 horas durante 48 horas.
A las 24 horas de realizado el procedimiento la tutora manifestó que el animal estaba incómodo, no apoyaba el miembro y vocalizaba evidenciando dolor al tocar la zona del pliegue craneal de la articulación del codo (húmero distal, radio y cúbito proximal) derecho. Se recomendó la aplicación de compresas frías y continuar con la analgesia, fue necesario un rescate analgésico que se realizó en el domicilio para el que se sumó firocoxib[5] a dosis de 5 mg/kg por día con el objetivo de que existiera una mejoría clínica inmediata. Transcurridos 5 días sin mejoría clínica, la tutora informó la aparición de una herida de gran tamaño sobre la cual aplicó un antiséptico doméstico con un colorante verdoso. Posteriormente concurrió a la clínica donde se evidenció la necrosis de la zona que era visible mediante una herida en forma de ocho en la zona del extremo del catéter infiltrado con externalización del extremo distal del músculo bíceps braquial.
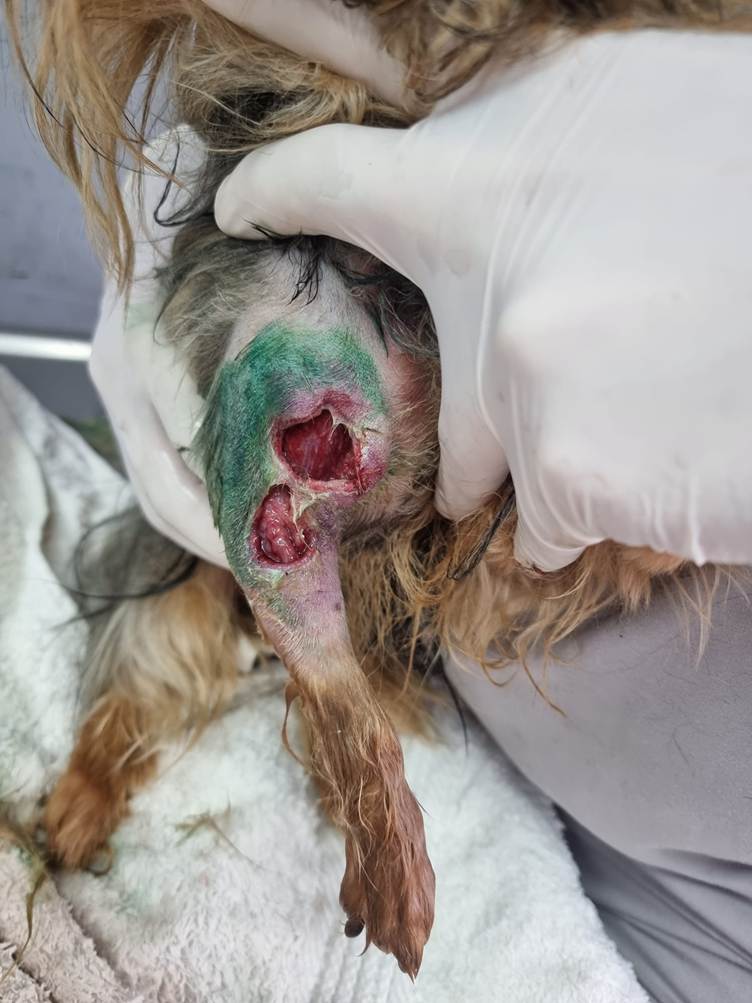
Figura 1: Día 5 de la extravasación de propofol, en la que se observa la ulceración de la piel y la necrosis tisular circundante, dejando en evidencia una herida en forma de ocho, con notoria exposición de los tejidos musculares
Se estableció un protocolo de manejo de heridas necrosadas y contaminadas, según Sopena et al. (2009), con el propósito de su cierre por segunda intención. Previo a esto, se extrajo una muestra de sangre para análisis y se realizó hemograma completo, funcional hepático, renal y glucemia, no se evidenciaron alteraciones. Lo primero que se realizó fue un desbridamiento quirúrgico del tejido necrosado bajo anestesia general con el mismo protocolo descrito antes y un lavado quirúrgico a presión con suero fisiológico y aguja 21G, para lo cual se adosó una llave de tres vías al extremo del infusor del suero, una jeringa de 20 ml y la aguja. Esto provocó la salida de una estructura tubular compatible con la vena cefálica necrosada. Luego del lavado, se aplicó crema con colagenasa y cloranfenicol[6] y se finalizó con un vendaje tipo Spica, en el cual se hace una pasada por el cuello para evitar desplazamientos del vendaje (Pavletic, 2011), realizado con gasas estériles, algodón laminado y vendas autoadherentes.[7]

Figuras 2 y 3: Vendaje compresivo realizado con gasas estériles, algodón laminado y vendas autoadhesivas, denominado vendaje de Spica
Se recomendó no interrumpir el antibiótico sugerido hasta evidenciar la presencia del tejido de granulación, por sus propiedades antibacterianas y antiinflamatorias, debido a la gran cantidad de neutrófilos, macrófagos y fibroblastos que posee y teniendo en cuenta a su vez que la espiramicina y el metronidazol es una asociación antibiótica que tiene utilidad en heridas de piel necrosadas (Papich, 2023).
El procedimiento de lavado con suero fisiológico se realizó a diario con jeringa y goteo suave sin necesidad de ejercer presión con aguja.
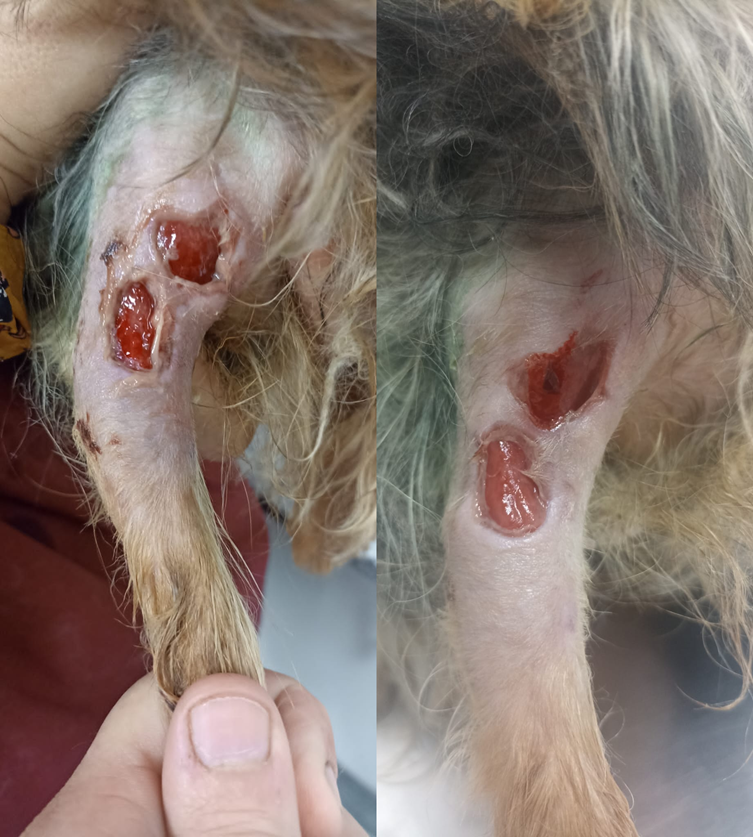
Figuras 4 y 5: Días 3 y 4 de la necrosis. Evolución de la herida exudativa en etapas tempranas
Tampoco fue necesaria la repetición de otro desbridamiento quirúrgico ni anestesias consecutivas. El tejido de granulación comenzó a formarse luego del cuarto día, se continuaron los lavados hasta que este cubrió toda la herida al séptimo día.
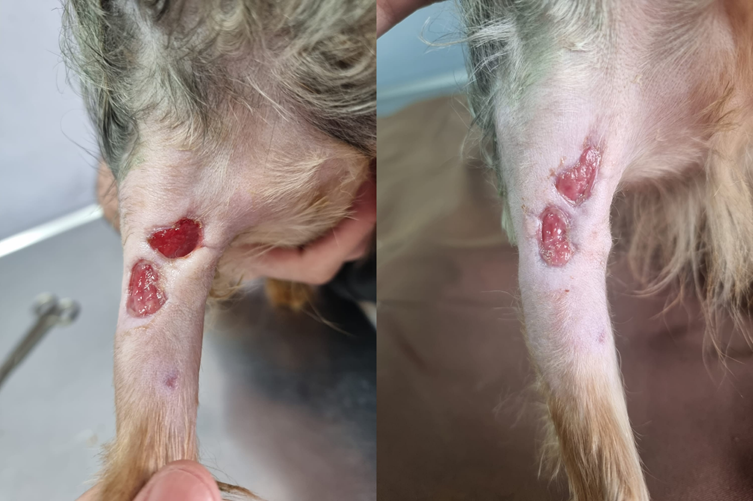
Figuras 6 y 7: Comienza a evidenciarse el tejido de granulación
Cuando el tejido de granulación fue abundante y de características saludables —hidratado y de color rosado, no se evidenció otro tipo de color que sugiriera infección— se indicó la interrupción de los antibióticos. Se continuó el manejo de la herida siempre bajo vendaje aplicando pomada con sulfadiazina de plata al 1 %[8] hasta evidenciar la epitelización total de la herida.
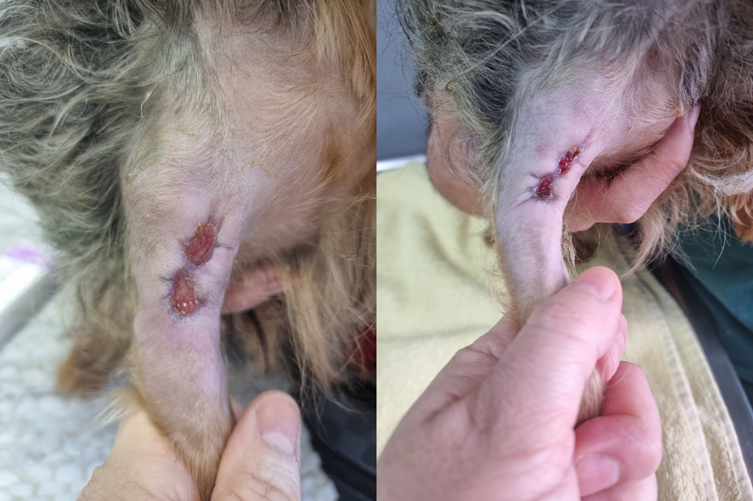
Figuras 8 y 9: Comienzo de la epitelización
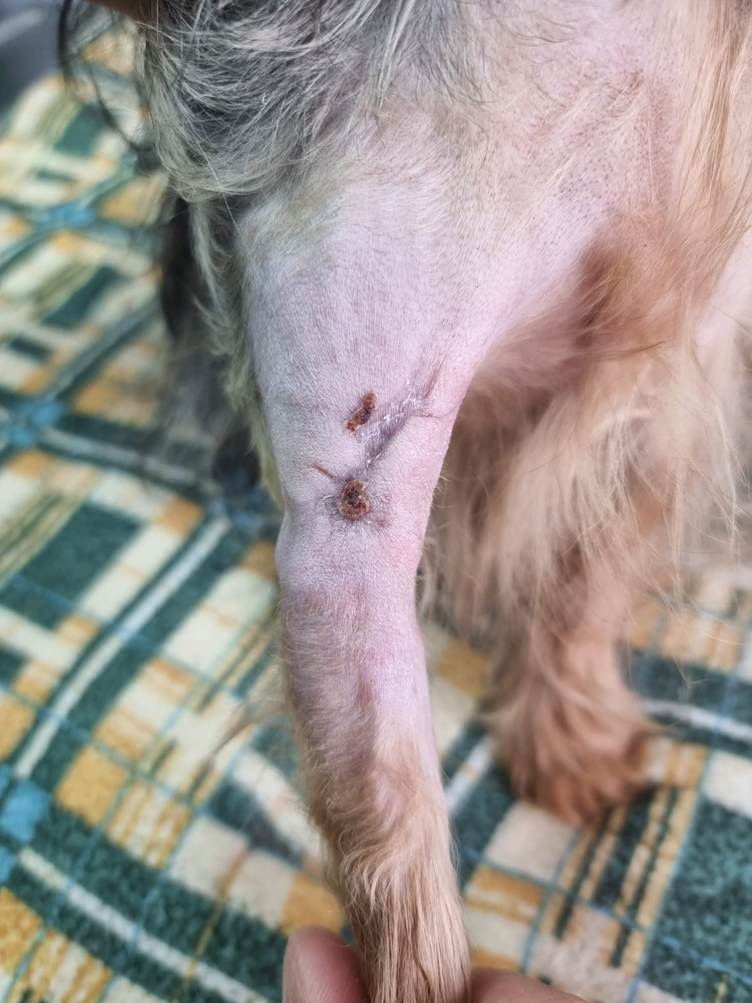
Figura 10: Día 12 desde la necrosis, cicatrización total de la herida y alta del paciente
Se finalizó cada procedimiento con el vendaje descrito antes.
El paciente evolucionó favorablemente el apoyo del miembro afectado y se dio de alta sin claudicación a los 12 días de la necrosis, controlándola a los 20 días.
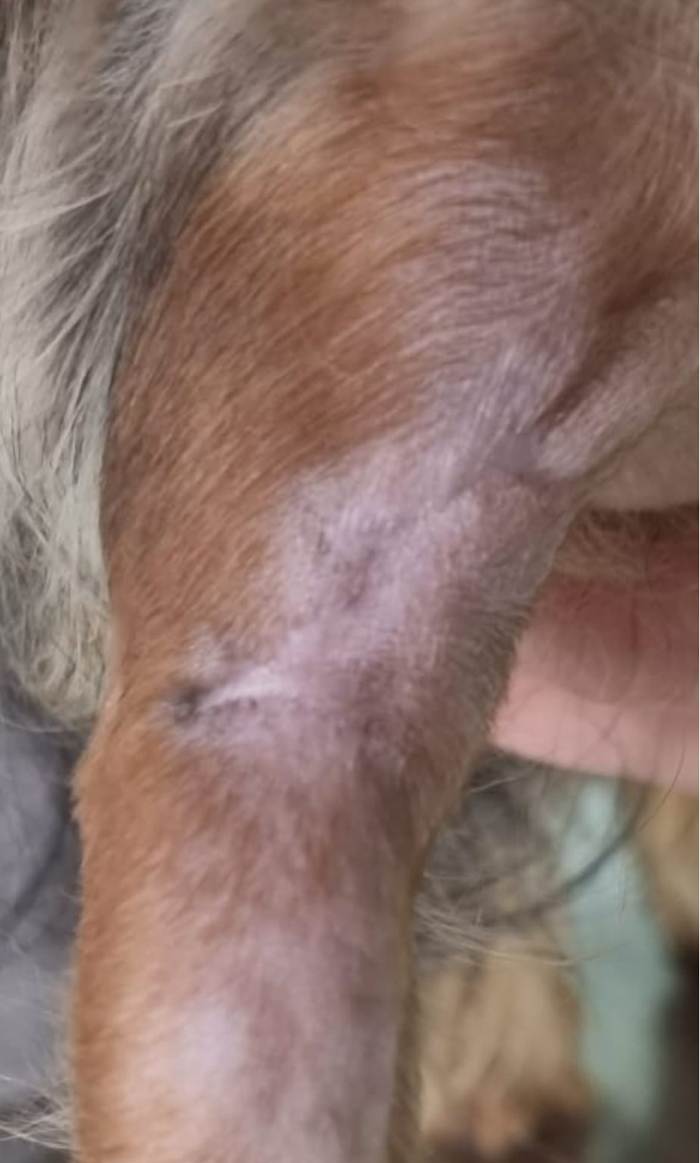
Figura 11: Día 20 desde la necrosis, control de la cicatrización. Se observa leve contracción de la cicatriz
Se observó una leve retracción de los bordes de la herida, que no ocasionaba incomodidad ni retracción muscular o disminución de la flexión ni extensión de la articulación del codo (húmero-tibio-cubital).
Discusión
En la práctica quirúrgica particular específica de la autora, que data de veinticinco años, y según relatos orales de otros profesionales, este tipo de necrosis nunca había sido observada hasta la fecha. Si bien la prevalencia es baja, la magnitud de las lesiones es significativa debido a la severidad y el dolor que le provocan al animal, lo que constituye una complicación anestésica local moderada. Si bien hay casos que no fueron reportados, se han comunicado heridas por desenguantado debido a la extravasación de propofol, similares a las citadas por extravasación de fluidoterapia o quimioterapia (Carrillo et al., 2015).
En este paciente se utilizaron drogas preanestésicas plausibles de provocar necrosis, pero se descartó su involucro, debido al escaso volumen inyectado según las dosis calculadas y por haber evidenciado el efecto deseado al momento de su pico máximo en sangre según su farmacocinética, constatando la correcta permeabilidad del catéter en ese momento.
Una vez advertida la infiltración de la vía de venoclisis, a pesar de que el animal no demostró incomodidad, se cambió inmediatamente, pero no se tomaron medidas específicas, como inyección de suero fisiológico o el enfriamiento de la zona, como lo detallan algunos autores (Shibata et al., 2016). Esto se debió a que se subestimó las consecuencias de la extravasación, debido a que frente eventos incluso peores no se habían evidenciado complicaciones. A pesar de lo anterior, se estima que el porte tan pequeño del animal y la delicadeza de sus tejidos agravaron el cuadro clínico.
En cuanto al tratamiento de elección, se pudo realizar un tratamiento convencional para el manejo de heridas sin necesidad de requerir de intervenciones quirúrgicas posteriores ni la aplicación de otro tipo de tratamientos que podrían haber sido necesarios debido a posibles complicaciones en la cicatrización, que no existieron en este paciente. Si bien en este paciente dio buenos resultados el uso de estas pomadas y los vendajes utilizados, se podría haber sumado el uso de parches con antibióticos durante los primeros días, una vez constatada la necrosis, o la aplicación de plasma rico en plaquetas (PRP) o algún otro hemoderivado como la fibrina rica en plaquetas (PRF), para acelerar el proceso de cicatrización (Iacopetti et al., 2020).
Conclusiones
La extravasación de propofol ocasionó una complicación mediata local moderada que provocó la necrosis de piel y tejido subcutáneo en este paciente canino, se logró la cicatrización total de la piel, sin complicaciones, mediante un manejo básico de heridas.
Agradecimientos
A la tutora de Mirko, quien se mostró colaborativa y aceptó compartir generosamente el material fotográfico para su uso en medios de difusión académicos.
Referencias
Bohling, M. W., & Henderson, R. A. (2006). Differences in cutaneous wound healing between dogs and cats. Veterinary Clinics of North America: Small Animal Practice, 36(4), 687-692. https://doi.org/10.1016/j.cvsm.2006.02.001
Carillo, J.M., Cava, P., Zuriaga, E., & Rubio, M. (2015). Herida por extravasación de la fluidoterapia. En J.J. Sopena Juncosa (Ed.), Casos clínicos de cirugía de la piel (pp. 136- 147). Servet.
Errante, P. R. (2023). Extravasation injuries in the intravenous therapy with drugs with properties vesicants and irritants in the veterinary medicine of small animals. Journal of Dairy Veterinary and Animal Research, 12(1), 19-22. https://doi.org/10.15406/jdvar.2023.12.00317
Fischer, B. L., & Martin-Flores, M. (2024). Complications associated with locoregional anesthesia. En M. Read, L. Campoy & B. Fischer (Eds.), Small animal regional anesthesia and analgesia (2.ª ed., pp. 267-286). Wiley. https://doi.org/10.1002/9781119514183.ch28
Flancman, R., Singh, A., & Weese, J. S. (2018). Evaluation of the impact of dental prophylaxis on the oral microbiota of dogs. PLOS ONE, 13(6), e0199676. https://doi.org/10.1371/journal.pone.0199676
Garrigues, F., Martínez, A., & Pérez, L. (2019). Guía de manejo en la extravasación de medicamentos no citotásticos. CIM.
Grubb, T., Sager, J., Gaynor, J. S., Montgomery, E., Parker, J. A., Shafford, H., & Tearney, C. (2020). 2020 AAHA Anesthesia and monitoring guidelines for dogs and cats. Journal of the American Animal Hospital Association, 56(2), 59-82. https://doi.org/10.5326/JAAHA-MS-7055
Iacopetti, I., Patruno, M., Melotti, L., Martinello, T., Bedin, S., Badon, T., Righetto, E. M., & Perazzi, A. (2020). Autologous platelet-rich plasma enhances the healing of large cutaneous wounds in dogs. Frontiers in Veterinary Science, 7, 575449. https://doi.org/10.3389/fvets.2020.575449
Le, A., & Patel, S. (2014). Extravasation of noncytotoxic drugs. Annals of Pharmacotherapy, 48(7), 870-886. https://doi.org/10.1177/1060028014527820
Mahajan, R., Gupta, R., & Sharma, A. (2006). Extravasation injury caused by propofol. Anesthesia & Analgesia, 102(2), 648. https://doi.org/10.1213/01.ane.0000190745.29994.58
Minghella, M. S., Smith, J. A., & Johnson, L. K. (2010). Pain after injection of a new formulation of propofol in six dogs. Veterinary Record, 167, 866-867. https://doi.org/10.1136/vr.c5736
Otero, P. E. (2012). Protocolos anestésicos y manejo del dolor en pequeños animales. Inter-Médica.
Papich, M. G. (2023). Antimicrobial agents in small animal dermatology for treating staphylococcal infections. Journal of the American Veterinary Medical Association, 261(S1), S130-S139. https://doi.org/10.2460/javma.23.01.0023
Pavletic, M. M. (2011). Apósitos, vendajes, sostén externo y dispositivos para protección. En Atlas de manejo de la herida y cirugía reconstructiva en pequeños animales (3.ª ed., pp. 79-107). Wiley-Blackwell.
Shibata, M., Nakajima, K., & Kimura, T. (2016). Injury due to extravasation of thiopental and propofol: Risks/effects of local cooling/warming in rats. Biochemistry and Biophysics Reports, 8, 207-211. https://doi.org/10.1016/j.bbrep.2016.09.005
Simpson, S. E., & Zersen, K. M. (2022). Incidence and type of peripheral intravenous catheter complications documented in hospitalised dogs. Journal of Small Animal Practice, 64(3), 130-135. https://doi.org/10.1111/jsap.13574
Sopena, J., Martínez, R., & López, M. (2009). Manejo de heridas y principios de cirugía plástica en pequeños animales. Servet.
Vasquez, M. P., Daly, M., Boyd, C. J., Crandell, D. E., Hall, K. E., Mays, E. L., Ngwenyama, T., Ortolani, J., Smith, M.R., Hoehne, S.N., Martin, L., & Davidow, E. B. (2025). Multicenter retrospective evaluation of norepinephrine extravasation in dogs and cats (2015-2021): 14 cases. Journal of Veterinary Emergency and Critical Care, 35(1), 73-80. https://doi.org/10.1111/vec.13442
Nota de contribución
Claudia de Aurrecoechea ha colaborado en 1, 2, 3, 4, 5, 6, 7, 8.
Ignacio Fagúndez en 2, 3, 5.
Declaración de uso de IA
Los autores usaron y supervisaron el uso de la herramienta ChatGPT para cotejar la traducción al inglés y al portugués.
Nota del editor
El editor José Manuel Verdes aprobó este artículo.