Veterinaria (Montevideo), 2026 62(225), https://doi.org/10.29155/VET.62.225.3
Artículo original
Distemper canino en Uruguay: diagnóstico molecular y caracterización filogenética de cepas circulantes (2021-2023)
Canine Distemper in Uruguay: molecular diagnosis and phylogenetic characterization of circulating strains (2021-2023)
Cinomose Canina no Uruguai: diagnóstico molecular e caracterização filogenética de cepas circulantes (2021-2023)
Victoria Iribarnegaray1 https://doi.org/0000-0002-0245-9152
Guillermo Godiño2 https://doi.org/0009-0005-4514-1944
José Manuel Verdes2 https://doi.org/0000-0003-4314-906X
Rodrigo Puentes1 https://doi.org/0000-0002-4618-9721
1Unidad Académica de Microbiología, Departamento de Patobiología, Facultad de Veterinaria, Universidad de la República, Montevideo, Uruguay. Autor para correspondencia: victoria.iribarnegaray@pedeciba.edu.uy
2Unidad Académica de Patobiología, Departamento de Patobiología, Facultad de Veterinaria, Universidad de la República, Montevideo, Uruguay.
Cómo citar este artículo:
Iribarnegaray, V., Godiño, G., Verdes, J. M., & Puentes, R. (2026). Distemper canino en Uruguay: diagnóstico molecular y caracterización filogenética de cepas circulantes (2021-2023). Veterinaria (Montevideo), 62(225), e20266222503. https://doi.org/10.29155/VET.62.225.3
Resumen
El virus del distemper canino (CDV) es una infección vírica muy contagiosa que causa inmunosupresión y afecta cánidos domésticos y salvajes con una elevada mortalidad. Este estudio analizó retrospectivamente casos diagnosticados de CDV remitidos al Laboratorio de Diagnóstico Microbiológico de la Facultad de Veterinaria de la Universidad de la República (Montevideo, Uruguay) entre 2021 y 2023. Se procesaron 251 muestras, sobre todo de Montevideo (85 %) y se detectó CDV en 119 mediante RT-qPCR. No hubo diferencias significativas por sexo, y los caninos menores de 2 años fueron más susceptibles (71,4 %). Un 60 % de los casos no estaban vacunados, mientras que un 28 % presentaban plan de vacunación completo, lo que sugiere posibles fallas vacunales. Los caninos mestizos fueron los más afectados, pero el CDV se detectó en varias razas. Los signos principales fueron nerviosos, seguidos por respiratorios, digestivos y dermatológicos; un 24 % presentó signos combinados. El análisis filogenético sugiere un linaje predominante de CDV en Uruguay, con algunas cepas divergentes. Comprender la epidemiología y la presentación clínica del CDV en Uruguay es fundamental para mejorar las estrategias de prevención, diagnóstico y tratamiento.
Palabras clave: Distemper canino, Diagnóstico molecular, Epidemiología.
Abstract
The canine distemper virus (CDV) is a highly contagious viral infection that causes immunosuppression and affects domestic and wild canines with high mortality. This study retrospectively analyzed diagnosed CDV cases referred to the Microbiological Diagnostic Laboratory of the Faculty of Veterinary Medicine of Universidad de la República (Montevideo, Uruguay) between 2021 and 2023. A total of 251 samples were processed, mainly from Montevideo (85 %), with CDV detected in 119 using RT-qPCR. There were no significant differences by sex, and canines under 2 years old were more susceptible (71.4 %). Sixty percent of the cases were unvaccinated, while 28 % had a complete vaccination plan, suggesting possible vaccine failures. Mixed-breed canines were the most affected, but CDV was detected in several breeds. The main signs were neurological, followed by respiratory, digestive, and dermatological; 24 % presented combined signs. Phylogenetic analysis suggests a predominant CDV lineage in Uruguay, with some divergent strains. Understanding the epidemiology and clinical presentation of CDV in Uruguay is crucial for improving prevention, diagnosis, and treatment strategies.
Keywords: Canine distemper virus, Molecular diagnosis, Epidemiology.
Resumo
O vírus da cinomose canina (CDV) é uma infecção viral altamente contagiosa que causa imunossupressão e afeta cães domésticos e selvagens com alta mortalidade. Este estudo analisou retrospectivamente casos diagnosticados de CDV remetidos ao Laboratório de Diagnóstico Microbiológico da Faculdade de Veterinária da Universidad de la República (Montevidéu, Uruguai) entre 2021 e 2023. Foram processadas 251 amostras, principalmente de Montevidéu (85 %), com CDV detectado em 119 por meio de RT-qPCR. Não houve diferenças significativas por sexo, e os cães menores de 2 anos foram mais suscetíveis (71,4 %). Sessenta por cento dos casos não estavam vacinados, enquanto 28 % tinham um plano de vacinação completo, sugerindo possíveis falhas vacinais. Os cães mestiços foram os mais afetados, mas o CDV foi detectado em várias raças. Os sinais principais foram neurológicos, seguidos por respiratórios, digestivos e dermatológicos; 24 % apresentaram sinais combinados. A análise filogenética sugere uma linhagem predominante de CDV no Uruguai, com algumas cepas divergentes. Compreender a epidemiologia e a apresentação clínica do CDV no Uruguai é fundamental para melhorar as estratégias de prevenção, diagnóstico e tratamento.
Palavras-chave: Cinomose canina, Diagnóstico molecular, Epidemiologia.
Fecha de recibido: 27/03/2025
Fecha de aceptado: 27/10/2025
Introducción
El virus del distemper canino (CDV), enfermedad de Carré o joven edad, pertenece al género Morbillivirus (familia Paramyxoviridae) (Maes et al., 2019). El CDV presenta un genoma de ARN monocatenario de polaridad negativa, con nucleocápside helicoidal, rodeada de una envoltura lipoproteica que contiene proteínas como hemaglutinina (H), de fusión (F) y de matriz (M), las que participan en los mecanismos de infección, replicación viral y determinan el tropismo (Diallo, 1990; Örvell & Norrby, 1980). El CDV tiene la capacidad de infectar una amplia gama de especies y representa un riesgo para la conservación de la vida silvestre libre y cautiva en todo el mundo (Loots et al., 2017; Martínez-Gutiérrez & Ruiz-Saenz, 2016). En caninos domésticos, el CDV es una de las enfermedades virales de mayor incidencia con altas tasas de morbilidad y mortalidad (Summers & Appel, 1994). Los animales de todas las edades y razas son susceptibles a la infección por el CDV. Sin embargo, los animales no vacunados o los que han desarrollado inmunidad incompleta son los más predispuestos a enfermarse (Ettinger & Feldman, 2010). La prevalencia de CDV en caninos se incrementa entre 3 a 6 meses de edad, correlacionándose con la caída de anticuerpos maternales en cachorros (Ettinger & Feldman, 2010). El desarrollo de la enfermedad y los signos clínicos son muy variables y dependen principalmente de la edad, el estado inmunitario, la historia previa de vacunación, así como la virulencia de la cepa (Beineke et al., 2009; Lempp et al., 2014). El tracto gastrointestinal y los sistemas respiratorio y nervioso son los más afectados en todas las especies (da Fontoura Budaszewski et al., 2016; Loots et al., 2017). En lo que respeta al tratamiento, no existe un tratamiento antiviral efectivo, lo que se utiliza son medidas paliativas de sostén, dirigidas a limitar la invasión bacteriana secundaria mediante la utilización de antibióticos de amplio espectro, apoyando el equilibrio de líquidos y en caso de problemas respiratorios, expectorantes y broncodilatadores (Ettinger & Feldman, 2007). La mejor forma de prevención de la enfermedad es mediante la vacunación, y en ese sentido el desarrollo y utilización de las vacunas contra el CDV se ha empleado desde la década del cincuenta. Desde esa fecha a la actualidad se ha observado una drástica disminución en la aparición de casos de CDV, sin embargo, se han detectados brotes de la enfermedad en diferentes regiones del mundo en animales inmunizados (Calderón et al., 2007; Gemma et al., 1996; Lan et al., 2006; Martella et al., 2008; Radtanakatikanon et al., 2013).
El diagnóstico oportuno y preciso del CDV es crucial para la atención y tratamiento de los caninos infectados, así como para prevenir la propagación de la enfermedad en poblaciones susceptibles. Aunque los hallazgos clínicos pueden ser útiles para una sospecha inicial, no son suficientes para confirmar la infección (Fischer et al., 2013; Saito et al., 2006). En este contexto, los avances en las metodologías diagnósticas han permitido la implementación de técnicas más sensibles y específicas para la detección de CDV, como la PCR en tiempo real (RT-qPCR), la digital PCR y la prueba inmunocromatográfica rápida, entre otras (Athanasiou et al., 2018; Iribarnegaray et al., 2024; Temilade et al., 2015). Estas metodologías, al ser rápidas, rentables y de fácil acceso, han transformado el diagnóstico del CDV permitiendo detectar el virus incluso en casos con cargas virales bajas o en fases tempranas de la enfermedad (Fischer et al., 2013; Iribarnegaray et al., 2024).
En este artículo, se presenta una descripción de la casuística del virus de distemper canino en el laboratorio de Diagnóstico Microbiológico de la Facultad Veterinaria, Udelar, de Montevideo, Uruguay. Para ello se analizaron retrospectivamente las características epidemiológicas y clínicas de los casos confirmados mediante RT-qPCR entre los años 2021 y 2023. El principal objetivo de este trabajo es proporcionar información relevante para la comprensión de la distribución y la evolución de la enfermedad en el país, así como para optimizar las estrategias diagnósticas y de control.
Materiales y métodos
Muestras biológicas
Este estudio se basó en el análisis de 251 muestras obtenidas del Hospital de la Facultad de Veterinaria (n=63) y de clínicas veterinarias privadas de Uruguay (n=188), recolectadas entre 2021 y 2023.
Las muestras incluyeron orina (n=61), sangre (n=115), secreciones nasales y oculares (n=49), líquido cefalorraquídeo (LCR) (n=4) y cerebelo (n=22). El tipo de muestra recolectada fue determinado por el médico veterinario según las recomendaciones específicas para cada fase de la enfermedad (Martella et al., 2008; Sarchahi et al., 2022). Además, se recopilaron datos epidemiológicos, como edad, sexo, raza, estado de vacunación y signos clínicos presentes. Todas las muestras fueron almacenadas a −80 °C hasta su procesamiento. Los protocolos experimentales correspondientes fueron revisados y aprobados por la Comisión de Ética en el Uso de Animales (CEUA) de la Facultad de Veterinaria, Universidad de la República (número de aprobación CEUAFVET-1003/20; Exp. 111900-000900-20).
Extracción de ARN y síntesis de cDNA
La extracción de ARN a partir de orina, sangre, secreciones nasales y oculares y LCR se realizó siguiendo las recomendaciones del kit comercial RNA viral kit (Zymo Research, Irvine, CA). Para las muestras de cerebelo, se emplearon 30 mg de tejido y se utilizó el método TRIzol (Zymo Research, USA), siguiendo las instrucciones del fabricante.
El ARN total fue tratado con ADNasa I (Invitrogen, Carlsbad, CA) para eliminar posibles contaminaciones de ADN genómico. Posteriormente, la síntesis del ADNc se llevó a cabo con el kit SensiFAST cDNA (Bioline, UK), de acuerdo con las indicaciones del fabricante. El ADNc obtenido se almacenó a −20 °C hasta su uso.
Detección del genoma viral mediante PCR cuantitativa con transcriptasa inversa en tiempo real (RT-qPCR)
La detección del genoma viral en las muestras se llevó a cabo mediante RT-qPCR, amplificando un fragmento de 89 pb del gen N que codifica para la nucleoproteína (NP) con los cebadores CDV-RV: ´FAM-TGGCATTGAAACTATGTATCCGGCTCT-BHQ1-3´, y las secuencias de los primers fueron CDV-forward: 5´AGCTAGTTTCATCCTAACTATCAAGT3´ (Forward) y CDV-reverse: 5´ATGAGTTTTCCGGAGAATTAACAA3´ (Reverse) (Iribarnegaray et al., 2024). Para cada reacción de amplificación, se añadieron 1 μL de ADNc a una mezcla de reacción que contenía 10 μL de oasig™ lyophilized 2×qPCR Mastermix (Genesig®, Chandler’s Ford Eastleigh, Reino Unido), 1,2 μL de cebadores y sonda marcada con FAM (600 nM/300 nM) y agua ultra pura hasta completar el volumen final de 20 μL. La amplificación se llevó a cabo en un Corbett Rotor-Gene 3000 (Qiagen, ME, Alemania) bajo las siguientes condiciones de ciclado térmico: 2 minutos a 95 °C para la activación de la polimerasa y desnaturalización del ADN, seguidos de 50 ciclos de desnaturalización a 95 °C durante 10 segundos, y un paso de alineamiento/extensión con lectura de placa a 60 °C durante 60 segundos. Cada muestra se procesó por duplicado y se incluyeron dos controles sin ADN en todas las corridas. Los valores de Cq y los análisis de las curvas de calibración obtenidas a partir de diluciones seriadas en base diez del plásmido estándar fueron generados mediante Rotor-Gene AssayManager (Qiagen, ME, Alemania). Para cada uno de los tres ensayos independientes de RT-qPCR se aplicó una regresión lineal, calculándose el coeficiente de correlación (R²) y la eficiencia de amplificación (E%), determinada según la fórmula E% = (10^(-1/slope) − 1) × 100 (Iribarnegaray et al., 2024).
Preparación del plásmido
El ADN plasmídico utilizado para la generación de las curvas estándar se preparó mediante diluciones seriadas en base diez. La región objetivo, comprendida entre las posiciones 905 y 963 del gen que codifica la proteína de la nucleocápside (N), fue amplificada y clonada en el vector pGEM®-T Easy (Promega, Madison, WI, USA). Posteriormente, el vector recombinante se transformó en células competentes de Escherichia coli TOP10, las cuales se sembraron en placas de LB suplementadas con ampicilina, IPTG y X-Gal, incubándose durante la noche a 37 °C. Las colonias correspondientes a E. coli con el inserto viral fueron seleccionadas para su crecimiento en caldo LB. El plásmido recombinante se extrajo utilizando el kit Plasmid Mini (Zymo Research, Irvine, CA, USA) y se almacenó a −20 °C hasta su uso. La presencia y orientación del inserto se confirmaron mediante PCR y secuenciación (Macrogen, Seúl, República de Corea). La concentración de ADN plasmídico se determinó con un espectrofotómetro NanoDrop (Thermo Fisher Scientific, Wilmington, DE, USA) y se expresó como número de copias por microlitro.
Análisis filogenético
Se realizaron análisis filogenéticos basados en la secuencia codificante péptido señal fsp del gen que codifica para la proteína de fusión (F), con un tamaño de amplicón de 405 pb. Varios estudios han demostrado que esta región posee gran variabilidad, siendo un adecuado marcador para clasificar las cepas de CDV (Lee et al., 2010; Sarute et al., 2013; Sultan et al., 2009). Para ello se utilizaron un total de 67 secuencias, de las cuales 24 correspondieron a muestras positivas seleccionadas aleatoriamente y 43 fueron secuencias de referencia recuperadas de GenBank (tabla 1, material suplementario I), representativas, como cepas vacunales y cepas de la región (Argentina, Brasil, Ecuador). Las secuencias fueron alineadas utilizando el programa MUSCLE (Multiple Sequence Comparison by Log-Expectation), que permite generar alineamientos múltiples de alta precisión y rendimiento (Edgar, 2004). El alineamiento múltiple se realizó con ClustalW2, y el análisis filogenético se llevó a cabo mediante el método Neighbor-Joining (NJ), considerando el modelo de Kimura. Finalmente, se construyó un árbol filogenético utilizando el método de máxima verosimilitud, con un análisis de bootstrapping basado en 1000 réplicas para evaluar la robustez de las ramas filogenéticas (European Bioinformatics Institute, 2024).
Procesamiento de datos y análisis estadístico
Los datos clínicos de las muestras positivas detectadas por RT-qPCR fueron analizados utilizando el software Rstudio (versión 2024.04.2+764; PBC, MA, USA). Se evaluaron diferencias en la incidencia de casos positivos entre estaciones del año mediante la prueba de chi-cuadrado. Asimismo, se comparó la distribución de casos positivos según la edad mediante un test de chi-cuadrado y se realizaron análisis de correlación entre edad y estado de vacunación. Los gráficos fueron generados con GraphPad Prism (versión 7.00, MA, USA).
Resultados
Durante el período comprendido entre 2021 y 2023, se remitieron un total de 251 muestras con sospecha de infección por CDV al Laboratorio de Diagnóstico Microbiológico de la Facultad de Veterinaria (Udelar). De estas, 119 (47 %) fueron confirmadas como positivas mediante RT-qPCR. El 85 % de las muestras correspondieron a la ciudad de Montevideo, mientras que las restantes provinieron de los departamentos de Maldonado (9 %), Lavalleja (3 %), Paysandú (1 %) y Colonia (2 %). Cabe detacar que la distribución geográfica observada en este estudio refleja principalmente la procedencia de las muestras remitidas al laboratorio de diagnóstico, ubicado en Montevideo. En consecuencia, la mayor concentración de casos provenientes de este departamento responde, en parte, a un sesgo geográfico asociado a la accesibilidad y cercanía del laboratorio. En 2021, se recibieron 95 muestras con signos clínicos compatibles con CDV, de las cuales 35 (36,8 %) resultaron positivas. En 2022, se procesaron 86 muestras, de las cuales 38 (44 %) resultaron positivas. Por último, en 2023, se analizaron 70 muestras, de las cuales 46 (65,7 %) fueron positivas. La incidencia de CDV aumentó significativamente a lo largo de los años, el estadístico de chi-cuadrado resultó ser X2=13,78, con un valor p<0,001, con un aumento notorio en el invierno de 2022. Las muestras con resultado positivo en la RT-qPCR (n=119) fueron incluidas en los análisis descriptivos, mientras que las muestras negativas fueron excluidas de los resultados que se presentan a continuación.
En cuanto a la incidencia de casos positivos según la estación del año, se realizó una prueba de chi-cuadrado para evaluar si existen diferencias significativas en la distribución de frecuencias entre las estaciones y los años. El estadístico de chi-cuadrado resultó ser X2=27,48 p<0,001, lo que indica que hay diferencias significativas en la distribución de frecuencias entre los años y estaciones (figura 1). En la comparación entre años, se encontraron diferencias significativas entre 2021 y 2022 (X2=23,45, p<0,001), así como entre 2022 y 2023 (X2=13,45 p<0,01), mientras que no hubo diferencias significativas entre 2021 y 2023. El año 2022 presentó la mayor variabilidad, especialmente debido a su alta frecuencia en invierno.
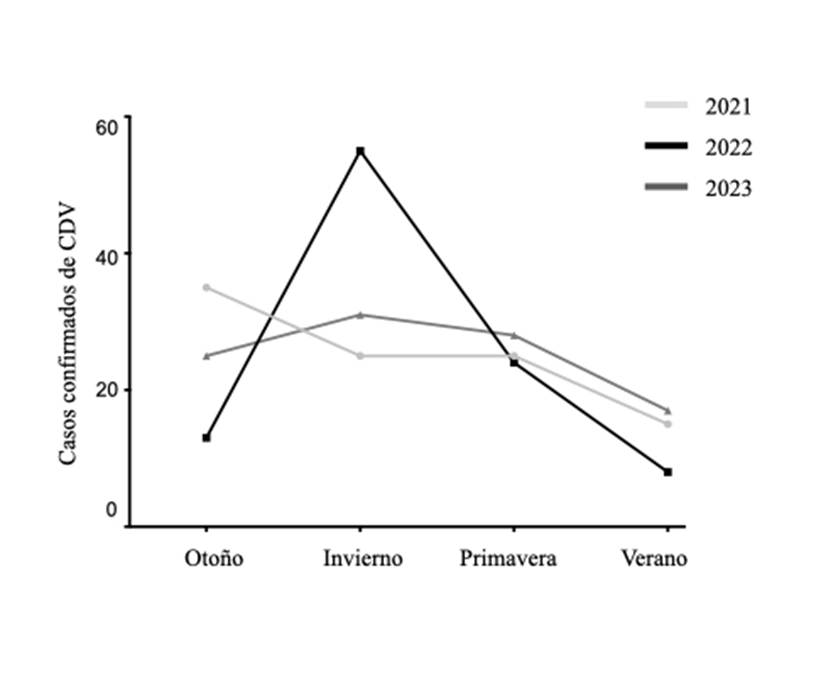
Figura 1: Distribución de casos confirmados mediante RT-qPCR del virus de distemper canino durante los años 2021-2023. En gris claro 2021, en negro 2022, en gris 2023, a lo largo de las estaciones
En la tabla 1 se presenta la distribución de casos positivos según el sexo, la edad y el estado de vacunación. La frecuencia de hembras (n=52) y machos (n=58) es similar. En cuanto a la edad, los caninos menores de 2 años representan el grupo con mayor incidencia, con un 71,4 %, (p≤0,0001), mientras que los de 3 a 7 años constituyen el 33 % y los mayores de 8 años el 20 %. En relación con el estado de vacunación, el 28 % (n=23) de los casos presentaban las vacunas al día, mientras que el 64 % no contaba con un esquema de vacunación actualizado. No observamos una relación significativa entre la vacunación y la edad en los casos positivos, para determinarlo se llevó a cabo una tabla de contingencia la cual incluyó tres categorías de edad (0-2 años, 3-7 años y mayores de 8 años) y dos categorías de vacunación (vacunados y no vacunados). El estadístico X2=1,75, con 2 grados de libertad y un valor p>0,05.
Tabla 1. Descripción de los casos positivos a CDV confirmados mediante RT-qPCR durante el 2021-2023 en Uruguay

Cabe destacar que, en muchos de los casos positivos, se enviaron dos o más tipos de muestras, por ejemplo, secreciones nasales y orina. De esta forma, en algunos casos, se evaluó la presencia de CDV en distintas muestras del mismo animal (figura 2).
Tabla 2: Descripción de las razas presentes en los casos positivos a CDV confirmados mediante RT-qPCR durante 2021-2023 en Uruguay

En cuanto a la distribución de casos positivos según la raza, se observó que los mestizos fueron los más representados en el estudio, con una incidencia del 46,8 % (tabla 2).
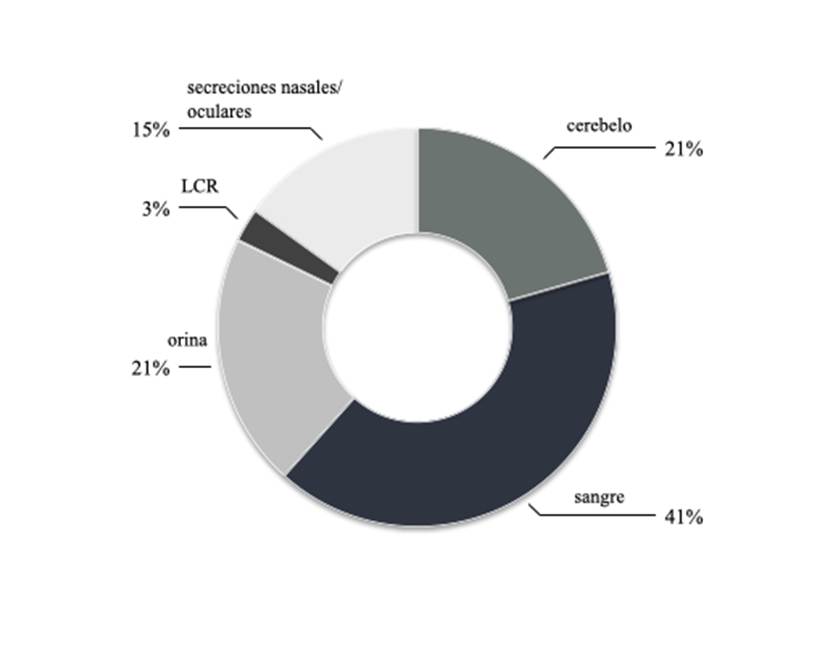
Figura 2: Muestras donde se detectó el CDV. Cerebelo (n=30), sangre (n=60), orina (n=30), LCR (líquido cefalorraquídeo) (n=4) y secreciones nasales y oculares (n=22)
En relación con los signos clínicos observados, el 54 % de los casos presentaron signos neurológicos, seguidos por signos respiratorios (20 %), digestivos (16 %) y dermatológicos (3 %). Al analizar los signos clínicos más representativos en cada categoría, se encontró que las mioclonías y convulsiones fueron los más comunes dentro de los signos neurológicos. En los signos respiratorios, la secreción ocular y nasal fueron los hallazgos más frecuentes. En cuanto a los signos digestivos, el vómito y la diarrea fueron los más reportados. En lo referente a los signos dermatológicos, solo se registró hiperqueratosis (figura 3). Por otra parte, el 24 % de los casos presentaron más de un tipo de signos clínicos, siendo la combinación de signos neurológicos y respiratorios la más frecuente.
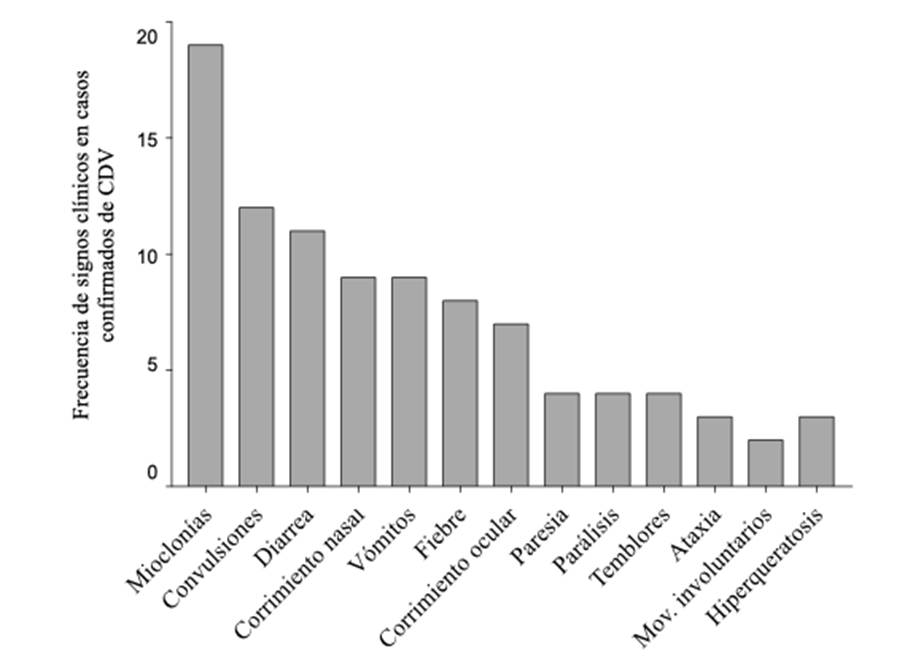
Figura 3: Descripción de frecuencias de los signos clínicos presentes en las muestras positivas a CDV
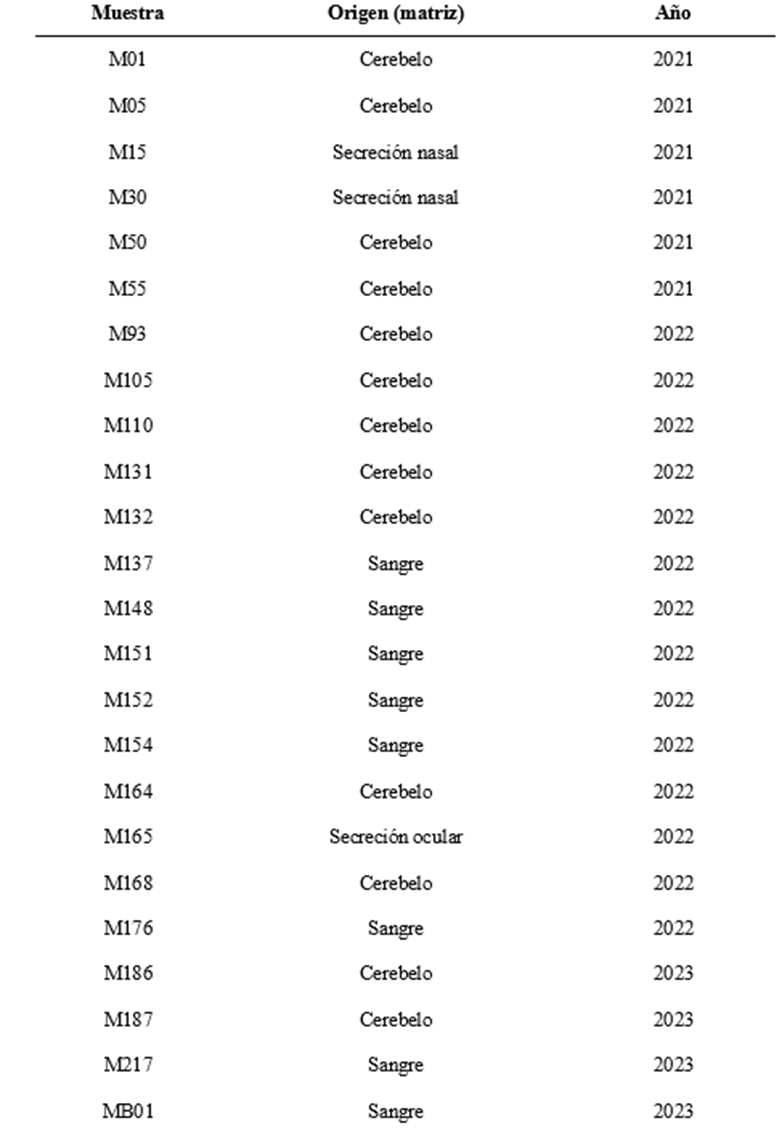
Del total de casos confirmados, se seleccionaron aleatoriamente 24 muestras positivas a CDV para amplificar la región fsp del gen F y construir la filogenia de las cepas. En la tabla 2 del material suplementario I, se detalla la información de las cepas, su origen y el año de muestreo. El análisis filogenético (figura 4) mostró que la mayoría de las muestras locales (azul) se agruparon en uno único (clúster), diferenciados de las cepas vacunales, con valores de soporte bootstrap elevados (superiores a 70). Dentro de estos clados locales se identificaron subdivisiones con soporte significativo, lo que refleja la existencia de posibles variantes de origen local. Dentro de los agrupamientos mayores, es posible identificar subgrupos internos que presentan soportes altos (bootstrap >85), como es el caso del subclado integrado por las muestras M15, M55, M98 y M50, lo que sugiere una relación filogenética cercana entre estos aislamientos y podría ser indicativo de transmisión local sostenida. Finalmente, las cepas vacunales (Onderstepoort, Snyder Hill y Lederle) formaron un clado externo, filogenéticamente distante de los aislamientos clínicos.
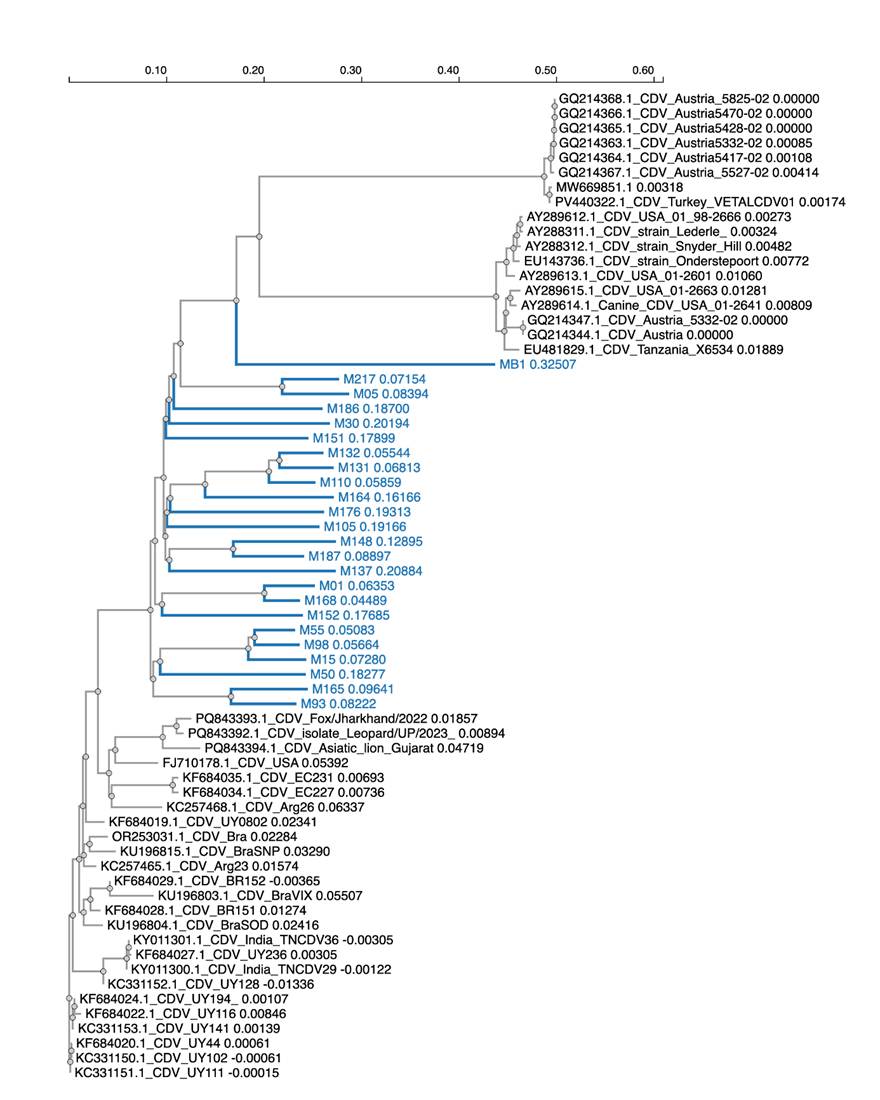
Figura 4: Árbol filogenético construido a partir del fragmento fsp del gen de la proteína de fusión (F) del CDV. Cepas locales (en azul), construcción mediante EMBL-EBI Job Dispatcher sequence analysis tools
Discusión
Los datos epidemiológicos obtenidos de las muestras procesadas con sospecha de CDV en el Laboratorio de Diagnóstico Microbiológico de la Facultad de Veterinaria (Udelar), Uruguay, entre 2021 y 2023, resaltan la continua relevancia del CDV como un problema significativo en salud canina. El número de casos confirmados (n=119) no solo refleja la persistencia del virus en la población canina, sino también la importancia de mejorar las estrategias de diagnóstico y prevención. Este hallazgo subraya la necesidad urgente de mantener una vigilancia continua, con un enfoque en la prevención a través de la vacunación y medidas de control más estrictas, dada la alta transmisibilidad del virus y sus efectos potencialmente letales en los caninos.
La incidencia de CDV aumentó de forma significativa a lo largo de los años (p>0,001) y se observa un aumento notorio en el invierno de 2022. Este aumento podría estar asociado a las condiciones climáticas, ya que el invierno de 2022 fue uno de los más fríos de los últimos 42 años, con una anomalía de temperatura media de −0,7 °C (Instituto Uruguayo de Meteorología (Inumet), 2022), lo cual podría haber favorecido la persistencia del virus en el ambiente y un incremento en la vulnerabilidad de los caninos ante las bajas temperaturas. Además, durante el período de 2021 a 2023, la población canina gradualmente comenzó a salir más a lugares públicos debido a la disminución de las restricciones por la pandemia de COVID-19. Este cambio en los comportamientos, con un aumento de la socialización y la interacción entre caninos en espacios abiertos, podría haber incrementado las oportunidades de exposición y transmisión del CDV, lo que a su vez podría haber influido en el aumento de casos observados en 2023. Aunque esta es una hipótesis que aún requiere más investigación, es un aspecto a considerar entre los factores asociados a la incidencia de la enfermedad.
El análisis de las fichas clínicas nos permitió constatar que no hay diferencia significativa en la incidencia de CDV según el sexo, lo que sugiere que el sexo no es un factor determinante en la susceptibilidad a la infección por CDV. Nuestros hallazgos concuerdan con otros estudios realizados en la región. Menezes et al. (2023), en Brasil, observaron frecuencias de infección similares entre machos (n=24) y hembras (n=22), sin encontrar una predisposición sexual significativa. De manera similar, Ariyama et al. (2024) reportaron frecuencias similares entre los sexos, siendo un 24 % (n=51) en hembras y 23 % (n=49) en machos, lo que refuerza la idea de que el virus afecta por igual a machos y hembras. Sin embargo, algunos estudios fuera de la región han reportado diferencias. Mousafarkhani et al. (2023), en Irán, encontraron una mayor susceptibilidad en hembras, aunque la tasa de mortalidad fue significativamente mayor en machos (p=0,024, OR=5,40, IC 95 %, 1,20-23,00). En contraste, en México, Rebollar-Zamorano et al. (2020) observaron que el 63 % (41 de 65) de los casos de CDV correspondían a machos. Estas discrepancias podrían deberse a variaciones en la dinámica local, como prácticas de manejo, acceso a atención veterinaria o factores genéticos que pueden influir en la resistencia al virus. Sin embargo, la consistencia de los resultados obtenidos en diferentes estudios regionales de América Latina, como los de Ariyama et al. (2024) y Menezes et al. (2023) fortalece la conclusión de que el sexo no juega un papel determinante en la susceptibilidad al CDV en la población canina en esta región.
La mayor susceptibilidad fue observada en los caninos menores de 2 años, los cuales representaron el 71,4 % del total de casos positivos. Este hallazgo coincide con estudios previos que establecen la vulnerabilidad asociada a la edad en la infección por CDV. Mousafarkhani et al. (2023) observaron que el 70 % de los casos positivos correspondían a caninos menores de 12 meses, con un 52,08 % de menos de 6 meses. De manera similar, en un estudio retrospectivo serológico, Leisewitz et al. (2001) observaron que la mayor incidencia de CDV se daba en cachorros menores a 1 año (19/34). Asimismo, Da Fontoura Budaszewski et al. (2014) encontraron que 71 de 155 animales afectados (45,8 %) tenían menos de 6 meses, 29 (18,7 %) estaban entre los 7 y 12 meses y 33 (21,3 %) tenían más de 1 año. Esta mayor susceptibilidad en los caninos más jóvenes podría ser atribuida a factores multifactoriales, derivándose tanto de un sistema inmunitario aún inmaduro como de la falta de un protocolo de vacunación completo o adecuado, lo que los hace más propensos a la infección.
La observación de que el 60 % de los casos confirmados de CDV carecían de registros de vacunación completos refuerza el papel crítico de la vacunación en la prevención de la enfermedad (Franco & Puentes, 2020; Larson & Schultz, 2006). Por otra parte, cabe destacar que el 28 % de los casos confirmados tenían esquemas de vacunación completos. Este hallazgo ha sido reportado en otros estudios, como el de Feijóo et al. (2021), quienes detectaron CDV en muestras de cerebelo de 4 caninos vacunados. De manera similar, Rebollar-Zamorano et al. (2020) observaron que 25 de los 65 caninos con diagnóstico confirmado de CDV presentaban un plan completo de vacunación al día. Por su parte, Menezes et al. (2023) reportaron que el 10,87 % (5/46) de los caninos infectados con CDV habían sido vacunados. La detección del virus en caninos vacunados puede atribuirse a varios factores. Uno de los principales es el fracaso de la vacuna, que puede deberse a la disminución de la inmunidad con el tiempo o la aparición de nuevas cepas del virus (Appel, 1978; Kapil et al., 2008). Además, el almacenamiento y la administración inadecuados de las vacunas también pueden comprometer su eficacia. La emergencia de nuevas variantes de CDV, como se ha observado en otros virus, podría superar la protección ofrecida por las vacunas actuales (Appel et al., 1978; Gámiz et al., 2011; Riley & Wilkes, 2015; Zhao et al., 2014). Estos desafíos destacan la necesidad de mejorar las estrategias de vacunación y monitorear constantemente la efectividad de las vacunas disponibles (Anis et al., 2018).
En cuanto a la raza, en el presente trabajo observamos un predominio de caninos mestizos entre los casos confirmados, lo cual puede reflejar la demografía de la población de caninos presentados para pruebas de diagnóstico, con una mayor proporción originaria de refugios u organizaciones de rescate. También cabe destacar que, según un estudio de Equipos Consultores de 2017, en el que se realizó un relevamiento sobre la población canina en Uruguay, se observó que los caninos mestizos eran los más frecuentes (47 % de 2 569 238 personas consultadas) en los hogares de los uruguayos, alcanzando un 51 % en la región metropolitana (Ministerio de Ganadería, Agricultura y Pesca (MGAP), 2017). Nuestros hallazgos son consistentes con estudios regionales, como el de Buñay Barahona (2019), quien reportó que la raza mestiza fue la más prevalente en su investigación (58,97 %, n=78); de igual forma, Da Fontoura Budaszewski et al. (2014), en Brasil, observaron una mayor incidencia en caninos mestizos (87/138), al igual que Menezes et al. (2023), donde los caninos mestizos representaron el 65,22 % (30/46) de los casos. Si bien los caninos mestizos fueron los más representados en el presente estudio, es importante tener en cuenta que el CDV se observó en varias razas, lo que enfatiza la amplia susceptibilidad de la población canina.
Los signos clínicos predominantes fueron los neurológicos (54 %), seguidos por los respiratorios (20 %), digestivos (16 %) y dermatológicos (3 %). Los signos neurológicos más comunes fueron mioclonías y convulsiones, lo cual coincide con lo reportado por varios autores, quienes describen la presencia de mioclonías como el signo predominante en los signos nerviosos (Feijóo, 2020; Koutinas et al., 2002; Silva et al., 2007). Las secreciones oculares y nasales fueron los signos más frecuentes dentro de los respiratorios; este tipo de manifestaciones es inespecífico, lo que puede confundirse con infecciones causadas por otros agentes virales, como el virus de la parainfluenza canina, el adenovirus canino tipo 2 (CAV-2) o el coronavirus respiratorio canino (CCoV) (Demeter et al., 2007). Dentro de los digestivos, los signos predominantes fueron vómitos y diarrea, mientras que la hiperqueratosis fue la principal manifestación dermatológica. Un 24 % de los casos presentó signos combinados, principalmente neurológicos y respiratorios. Esto refleja la naturaleza multisistémica del distemper, capaz de provocar lesiones en los sistemas respiratorio, gastrointestinal y neurológico (Beineke et al., 2009; Martella et al., 2008). La combinación de signos subraya la presentación variable de la enfermedad, lo que debe considerarse en cualquier canino enfermo.
El CDV presenta una diversidad genética significativa a nivel mundial, con varios linajes identificados. El linaje Europa está ampliamente distribuido y se encuentra en varias regiones, mientras que el linaje América se divide en subgrupos como América 1, América 2, América 3 y América 4, comúnmente asociados con cepas circulantes en el continente americano (Pinotti et al., 2016). Además, se ha identificado un linaje en Norteamérica, que muestra una divergencia significativa respecto a las cepas vacunales comunes (González Linares, 2015). En Sudamérica, se ha identificado una alta diversidad genética del CDV, con 4 linajes principales: Europa 1/South América 1, South América 2, South América 3 y South América 4 (Calderón et al., 2007; Espinal et al., 2014; Fischer et al., 2016; Panzera et al., 2012). En el presente estudio, se lograron obtener 24 secuencias de calidad suficiente y con la longitud adecuada para ser incluidas en el análisis filogenético. Desde el punto de vista molecular, las secuencias generadas a partir de la región fsp del gen F fueron obtenidas mediante la construcción de secuencias consenso, cuya calidad fue verificada por inspección de los histogramas. El análisis filogenético reveló que las cepas autóctonas se agrupan mayoritariamente junto a otras cepas uruguayas, pertenecientes al linaje Europa/South América 1, el cual incluye aislamientos del sur de Brasil, Uruguay, Argentina y países europeos. Estos resultados coinciden con lo descripto por Panzera et al. (2012). También observamos la existencia de subgrupos diferenciados entre las propias cepas locales, lo que podría estar relacionado con eventos de deriva genética o presión selectiva local. A diferencia de los aislamientos clínicos, las cepas vacunales formaron un clado monofilético distante, lo cual evidencia una divergencia filogenética considerable. Numerosos estudios han evidenciado que las cepas de campo del CDV presentan una alta diversidad genética y filogenética en comparación con las cepas vacunales clásicas, como Onderstepoort, Snyder Hill y Lederle, las cuales fueron aisladas entre las décadas de 1930 y 1950 y ya no circulan en poblaciones caninas domésticas (Anis et al., 2018; Demeter et al., 2007; Martella et al., 2011). Esta diferencia entre cepas vacunales y circulantes podría explicar algunos casos de falla vacunal reportados en la región y plantea la necesidad de evaluar la eficacia de las vacunas comerciales frente a variantes locales. Esos hallazgos resaltan la necesidad de realizar un estudio más completo de estas cepas, como la secuenciación del genoma completo, y subrayan la importancia de caracterizar la diversidad del CDV a nivel local para mejorar las estrategias de control de la enfermedad.
Conclusiones
Este estudio aporta información epidemiológica sobre el CDV en la población canina uruguaya. Se confirma la edad y el estado de vacunación como factores de riesgo clave, aunque la detección de CDV en animales vacunados resalta la necesidad de evaluar la eficacia de las vacunas y los protocolos de inmunización.
La presentación clínica predominante fue nerviosa, seguida por la respiratoria y digestiva, con casos de signos clínicos combinados.
A nivel molecular, la mayoría de las cepas analizadas pertenecen al linaje Europa/South América 1, aunque se identificaron variantes divergentes que sugieren la posible introducción de nuevas cepas o evolución local. Estos hallazgos destacan la importancia de la vigilancia epidemiológica y genética del virus para optimizar estrategias de control.
Agradecimientos
Agradecemos a los propietarios de las mascotas por su colaboración en la recolección de muestras, que contribuye al avance del conocimiento sobre el CDV en Uruguay. Asimismo, extendemos nuestro agradecimiento al Programa de Desarrollo de las Ciencias Básicas (Pedeciba), a la Comisión Académica de Posgrados (CAP) Udelar y a la Agencia Nacional de Investigación e Innovación (ANII) por el apoyo financiero a través del proyecto FMV-1-2019-1-155934, lo que permitió la realización de este estudio. Rodrigo Puentes y José Manuel Verdes son integrantes del Sistema Nacional de Investigadores (SNI, ANII) y docentes del Pedeciba.
Referencias
Anis, E., Newell, T. K., Dyer, N., & Wilkes, R. P. (2018). Phylogenetic analysis of the wild-type strains of canine distemper virus circulating in the United States. Virology Journal, 15(1), 118. https://doi.org/10.1186/s12985-018-1027-2
Appel, M. J. G. (1978). Reversion to virulence of attenuated canine distemper virus in vivo and in vitro. Journal of General Virology, 41(2), 385-393. https://doi.org/10.1099/0022-1317-41-2-385
Ariyama, N., Agüero, B., Bennett, B., Urzúa, C., Berrios, F., Verdugo, C., & Neira, V. (2024). Genetic characterization of Canine morbillivirus (Canine Distemper Virus) field strains in dogs, Chile, 2022-2023. Transboundary and Emerging Diseases, 2024(1). https://doi.org/10.1155/2024/9993255
Athanasiou, L. V., Kantere, M. C., Kyriakis, C. S., Pardali, D., Adamama Moraitou, K., & Polizopoulou, Z. S. (2018). Evaluation of a direct immunofluorescent assay and/or conjunctival cytology for detection of canine distemper virus antigen. Viral Immunology, 31(3), 272-275. https://doi.org/10.1089/vim.2017.0101
Beineke, A., Puff, C., Seehusen, F., & Baumgärtner, W. (2009). Pathogenesis and immunopathology of systemic and nervous canine distemper. Veterinary Immunology and Immunopathology, 127(1-2), 1-18. https://doi.org/10.1016/j.vetimm.2008.09.023
Buñay Barahona, T. G. (2019). Diagnóstico comparativo de moquillo en caninos (Canis lupus familiaris) machos y hembras mediante la técnica ELISA cuantitativa y ELISA cualitativa (Trabajo de titulación previo a la obtención del título, Universidad Politécnica Salesiana). Repositorio Institucional de la Universidad Politécnica Salesiana. https://dspace.ups.edu.ec/handle/123456789/17819
Calderón, M. G., Remorini, P., Periolo, O., Iglesias, M., Mattion, N., & La Torre, J. (2007). Detection by RT-PCR and genetic characterization of canine distemper virus from vaccinated and non-vaccinated dogs in Argentina. Veterinary Microbiology, 125(3-4), 341-349. https://doi.org/10.1016/j.vetmic.2007.05.020
da Fontoura Budaszewski, R., Pinto, L. D., Weber, M. N., Caldart, E. T., Alves, C. D., Martella, V., Ikuta, N., Lunge, V. R., & Canal, C. W. (2014). Genotyping of canine distemper virus strains circulating in Brazil from 2008 to 2012. Virus Research, 180, 76-83. https://doi.org/10.1016/j.virusres.2013.12.024
da Fontoura Budaszewski, R., Streck, A. F., Nunes Weber, M., Maboni Siqueira, F., Muniz Guedes, R. L., & Wageck Canal, C. (2016). Influence of vaccine strains on the evolution of canine distemper virus. Infection, Genetics and Evolution, 41, 262-269. https://doi.org/10.1016/j.meegid.2016.04.014
Demeter, Z., Lakatos, B., Palade, E. A., Kozma, T., Forgách, P., & Rusvai, M. (2007). Genetic diversity of Hungarian canine distemper virus strains. Veterinary Microbiology, 122(3-4), 258-269. https://doi.org/10.1016/j.vetmic.2007.02.001
Diallo, A. (1990). Morbillivirus group: genome organisation and proteins. Veterinary Microbiology, 23(1-4), 155-163. https://doi.org/10.1016/0378-1135(90)90145-L
Edgar, R. C. (2004). MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Research, 32(5), 1792-1797. https://doi.org/10.1093/nar/gkh340
Espinal, M. A., Díaz, F. J., & Ruiz-Saenz, J. (2014). Phylogenetic evidence of a new canine distemper virus lineage among domestic dogs in Colombia, South America. Veterinary Microbiology, 172(1-2), 168-176. https://doi.org/10.1016/j.vetmic.2014.05.019
Ettinger, S. J., & Feldman, E. C. (2007). Tratado de Medicina Interna Veterinaria. Elsevier.
Ettinger, S. J., & Feldman, E. C. (2010). Textbook of veterinary internal medicine. Elsevier Health Sciences.
European Bioinformatics Institute. (2024). https://www.ebi.ac.uk/Tools/
Feijóo, G. (2020). Distemper canino: seguimiento desde la presentación clínica hasta sus hallazgos histopatológicos e inmunohistoquímicos (Tesis de maestría, Facultad de Veterinaria, Universidad de la República). Colibrí. https://hdl.handle.net/20.500.12008/28621
Feijóo, G., Yamasaki, K., Delucchi, L., & Verdes, J. M. (2021). Central nervous system lesions caused by canine distemper virus in 4 vaccinated dogs. Journal of Veterinary Diagnostic Investigation, 33(4), 640-647. https://doi.org/10.1177/10406387211009210
Fischer, C. D. B., Gräf, T., Ikuta, N., Lehmann, F. K. M., Passos, D. T., Makiejczuk, A., Silveira, M. A. T., Jr, Fonseca, A. S. K., Canal, C. W., & Lunge, V. R. (2016). Phylogenetic analysis of canine distemper virus in South America clade 1 reveals unique molecular signatures of the local epidemic. Infection, Genetics and Evolution, 41, 135-141. https://doi.org/10.1016/j.meegid.2016.03.029
Fischer, C. D. B., Ikuta, N., Canal, C. W., Makiejczuk, A., Allgayer, M. da C., Cardoso, C. H., Lehmann, F. K., Fonseca, A. S. K., & Lunge, V. R. (2013). Detection and differentiation of field and vaccine strains of canine distemper virus using reverse transcription followed by nested real time PCR (RT-nqPCR) and RFLP analysis. Journal of Virological Methods, 194(1-2), 39-45. https://doi.org/10.1016/j.jviromet.2013.08.002
Franco, G., & Puentes, R. (2020). Pautas para la vacunación en caninos y felinos en Uruguay. Veterinaria (Montevideo), 56(213), e20202135605. https://doi.org/10.29155/VET.56.213.5
Gámiz, C., Martella, V., Ulloa, R., Fajardo, R., Quijano-Hernandéz, I., & Martínez, S. (2011). Identification of a new genotype of canine distemper virus circulating in America. Veterinary Research Communications, 35(6), 381-390. https://doi.org/10.1007/s11259-011-9486-6
Gemma, T., Watari, T., Akiyama, K., Miyashita, N., Shin, Y. S., Iwatsuki, K., Kai, C., & Mikami, T. (1996). Epidemiological Observations on Recent Outbreaks of Canine Distemper in Tokyo Area. Journal of Veterinary Medical Science, 58(6), 547-550. https://doi.org/10.1292/jvms.58.547
González Linares, A. B. (2015). Análisis genético y filogenético del gen de la hemaglutinina del virus del distemper canino (VDC) de cepas que circulan en el área metropolitana de Monterrey, N. L. (Tesis de maestría, Universidad Autónoma de Nuevo León). Repositorio Académico Digital. http://eprints.uanl.mx/id/eprint/15783
Instituto Uruguayo de Meteorología. (2022). Informe de invierno. Boletín trimestral, (3). https://www.inumet.gub.uy/sites/default/files/2022-09/Boletin%20estacional%20INVIERNO.pdf
Iribarnegaray, V., Godiño, G., Larrañaga, C., Yamasaki, K., Verdes, J. M., & Puentes, R. (2024). Droplet digital PCR enhances sensitivity of canine distemper virus detection. Viruses, 16(11), 1720. https://doi.org/10.3390/v16111720
Kapil, S., Allison, R. W., Johnston, L., Murray, B. L., Holland, S., Meinkoth, J., & Johnson, B. (2008). Canine distemper virus strains circulating among north american dogs. Clinical and Vaccine Immunology, 15(4), 707-712. https://doi.org/10.1128/CVI.00005-08
Koutinas, A. F., Polizopoulou, Z. S., Baumgaertner, W., Lekkas, S., & Kontos, V. (2002). Relation of clinical signs to pathological changes in 19 cases of canine distemper encephalomyelitis. Journal of Comparative Pathology, 126(1), 47-56. https://doi.org/10.1053/jcpa.2001.0521
Lan, N. T., Yamaguchi, R., Inomata, A., Furuya, Y., Uchida, K., Sugano, S., & Tateyama, S. (2006). Comparative analyses of canine distemper viral isolates from clinical cases of canine distemper in vaccinated dogs. Veterinary Microbiology, 115(1-3), 32-42. https://doi.org/10.1016/j.vetmic.2006.01.010
Larson, L. J., & Schultz, R. D. (2006). Effect of vaccination with recombinant canine distemper virus vaccine immediately before exposure under shelter-like conditions. Veterinary Therapeutics: Research in Applied Veterinary Medicine, 7(2), 113-118.
Lee, M. S., Tsai, K. J., Chen, L. H., Chen, C. Y., Liu, Y. P., Chang, C. C., Lee, S.H., & Hsu, W. L. (2010). The identification of frequent variations in the fusion protein of canine distemper virus. The Veterinary Journal, 183(2), 184-190. https://doi.org/10.1016/j.tvjl.2008.10.001
Leisewitz, A. L., Carter, A., Van Vuuren, M., & Van Blerk, L. (2001). Canine distemper infections, with special reference to South Africa, with a review of the literature: review article. Journal of the South African Veterinary Association, 72(3), 127-136. https://doi.org/10.4102/jsava.v72i3.635
Lempp, C., Spitzbarth, I., Puff, C., Cana, A., Kegler, K., Techangamsuwan, S., Baumgärtner, W., & Seehusen, F. (2014). New aspects of the pathogenesis of canine distemper leukoencephalitis. Viruses, 6(7), 2571-2601. https://doi.org/10.3390/v6072571
Loots, A. K., Mitchell, E., Dalton, D. L., Kotzé, A., & Venter, E. H. (2017). Advances in canine distemper virus pathogenesis research: a wildlife perspective. Journal of General Virology, 98(3), 311-321. https://doi.org/10.1099/jgv.0.000666
Maes, P., Amarasinghe, G. K., Ayllón, M. A., Basler, C. F., Bavari, S., Blasdell, K. R., Briese, T., Brown, P. A., Bukreyev, A., Balkema-Buschmann, A., Buchholz, U. J., Chandran, K., Crozier, I., de Swart, R. L., Dietzgen, R. G., Dolnik, O., Domier, L. L., Drexler, J. F., Dürrwald, R., … Kuhn, J. H. (2019). Taxonomy of the order Mononegavirales: second update 2018. Archives of Virology, 164(4), 1233-1244. https://doi.org/10.1007/s00705-018-04126-4
Martella, V., Elia, G., & Buonavoglia, C. (2008). Canine distemper virus. Veterinary Clinics of North America: Small Animal Practice, 38(4), 787-797. https://doi.org/10.1016/j.cvsm.2008.02.007
Martínez-Gutíerrez, M., & Ruiz-Saenz, J. (2016). Diversity of susceptible hosts in canine distemper virus infection: a systematic review and data synthesis. BMC Veterinary Research, 12(1), 78. https://doi.org/10.1186/s12917-016-0702-z
Menezes, K. M. F., Filho, G. D. de S., Damasceno, A. D., Souza, M., & Torres, B. B. J. (2023). Epizootiology of canine distemper in naturally infected dogs in Goiânia, Brazil. Ciência Rural, 53(8). https://doi.org/10.1590/0103-8478cr20220166
Ministerio de Ganadería, Agricultura y Pesca. (2017). Estudio sobre la población canina en Uruguay. https://www.gub.uy/ministerio-ganaderia-agricultura-pesca/datos-y-estadisticas/estadisticas/estudio-sobre-poblacion-canina-uruguay
Mousafarkhani, F., Sarchahi, A. A., Mohebalian, H., Khoshnegah, J., & Arbabi, M. (2023). Prevalence of canine distemper in dogs referred to Veterinary Hospital of Ferdowsi University of Mashhad, Mashhad, Iran. Veterinary Research Forum, 14(3), 153-160. https://doi.org/10.30466/vrf.2022.541661.3269
Örvell, C., & Norrby, E. (1980). Immunological relationships between homologous structural polypeptides of measles and canine distemper virus. Journal of General Virology, 50(2), 231-245. https://doi.org/10.1099/0022-1317-50-2-231
Panzera, Y., Calderón, M. G., Sarute, N., Guasco, S., Cardeillac, A., Bonilla, B., Hernández, M., Francia, L., Bedó, G., La Torre, J., & Pérez, R. (2012). Evidence of two co-circulating genetic lineages of canine distemper virus in South America. Virus Research, 163(1), 401-404. https://doi.org/10.1016/j.virusres.2011.10.008
Pinotti, M., Canavesio, M., Passeggi, C., Larrateguy, M. V., Paz, M., & Formentini, E. (2016). Virus de distemper canino: detección molecular de diferentes aislamientos provenientes de perros de la provincia de Santa Fe, Argentina, entre los años 2000 y 2010. InVet, 18(2), 349-355.
Radtanakatikanon, A., Keawcharoen, J., Charoenvisal, N. taya, Poovorawan, Y., Prompetchara, E., Yamaguchi, R., & Techangamsuwan, S. (2013). Genotypic lineages and restriction fragment length polymorphism of canine distemper virus isolates in Thailand. Veterinary Microbiology, 166(1-2), 76-83. https://doi.org/10.1016/j.vetmic.2013.05.015
Rebollar-Zamorano, M., Morales-Ubaldo, A. L., González-Alamilla, E. N., Ángeles-Rodríguez, A., Valladares-Carranza, B., Velásquez-Ordoñez, V., Rivero-Pérez, N., & Zaragoza-Bastida, A. (2020). Análisis epidemiológico retrospectivo de distemper canino en la ciudad de Pachuca de Soto, estado de Hidalgo. Journal of the Selva Andina Animal Science, 7(1), 40-46. https://doi.org/10.36610/j.jsaas.2020.070100040
Riley, M. C., & Wilkes, R. P. (2015). Sequencing of emerging canine distemper virus strain reveals new distinct genetic lineage in the United States associated with disease in wildlife and domestic canine populations. Virology Journal, 12(1), 219. https://doi.org/10.1186/s12985-015-0445-7
Saito, T. B., Alfieri, A. A., Wosiacki, S. R., Negrão, F. J., Morais, H. S. A., & Alfieri, A. F. (2006). Detection of canine distemper virus by reverse transcriptase-polymerase chain reaction in the urine of dogs with clinical signs of distemper encephalitis. Research in Veterinary Science, 80(1), 116-119. https://doi.org/10.1016/j.rvsc.2005.03.002
Sarchahi, A. A., Arbabi, M., & Mohebalian, H. (2022). Detection of canine distemper virus in cerebrospinal fluid, whole blood and mucosal specimens of dogs with distemper using RT‐PCR and immunochromatographic assays. Veterinary Medicine and Science, 8(4), 1390-1399. https://doi.org/10.1002/vms3.790
Sarute, N., Calderón, M. G., Pérez, R., La Torre, J., Hernández, M., Francia, L., & Panzera, Y. (2013). The fusion protein signal-peptide-coding region of canine distemper virus: a useful tool for phylogenetic reconstruction and lineage identification. PLoS One, 8(5), e63595. https://doi.org/10.1371/journal.pone.0063595
Silva, M. C., Fighera, R. A., Juliana S., B., Graça, D. L., Kommers, G. D., Irigoyen, L. F., & Barros, C. S. L. (2007). Aspectos clinicopatológicos de 620 casos neurológicos de cinomose em cães: Clinicopathological features in 620 neurological cases of canine distemper. Pesquisa Veterinária Brasileira, 27(5), 215-220. https://doi.org/10.1590/S0100-736X2007000500006
Sultan, S., Charoenvisal, N., Lan, N. T., Yamaguchi, R., Maeda, K., & Kai, K. (2009). The Asia 2 specific signal peptide region and other domains in fusion protein genes characterized Asia 1 and Asia 2 canine distemper viruses. Virology Journal, 6(1), 157. https://doi.org/10.1186/1743-422X-6-157
Summers, B. A., & Appel, M. J. G. (1994). Aspects of canine distemper virus and measles virus encephalomyelitis. Neuropathology and Applied Neurobiology, 20(6), 525-534. https://doi.org/10.1111/j.1365-2990.1994.tb01006.x
Temilade, B. E., Solomon, O. O. O., Omotayo, O. E., & Omezuruike, O. I. (2015). Seropositivity of canine distemper virus (CDV) in dogs presenting at Abeokuta, Nigeria. Public Health Research, 4, 109-119.
Zhao, J., Zhang, H., Bai, X., Martella, V., Hu, B., Sun, Y., Zhu, C., Zhang, L., Liu, H., Xu, S., Shao, X., Wu, W., & Yan, X. (2014). Emergence of canine distemper virus strains with two amino acid substitutions in the haemagglutinin protein, detected from vaccinated carnivores in North-Eastern China in 2012-2013. The Veterinary Journal, 200(1), 191-194. https://doi.org/10.1016/j.tvjl.2014.01.028
Nota de contribución
1. Conceptualización, 2. Curaduría de datos, 3. Análisis formal, 4. Investigación 5. Metodología, 6. Administración del proyecto, 7. Software, 8. Escritura - borrador original, 9. Escritura - revisión y edición, 10. Supervisión.
Victoria Iribarnegaray ha colaborado en 1, 2, 3, 8 y 9. Guillermo Godiño en 4 y 5. José Manuel Verdes en 1, 9 y 10. Rodrigo Puentes en 1, 9 y 10.
Disponibilidad de datos
El conjunto de datos que apoya los resultados de este estudio se encuentra disponible en la base de datos perteneciente al autor para correspondencia y se puede solicitar al correo electrónico victoria.iribarnegaray@pedeciba.edu.uy.
Nota del editor
La editora Analía Pérez aprobó este artículo.
Material suplementario I
Tabla 1: Secuencias obtenidas del GenBank

Tabla 2: Muestras seleccionadas para el estudio filogenético, donde se describe origen de la muestra y año de obtención